Vacinação de rotina em crianças pequenas
Noni E. MacDonald, MD, MSc FRCPc
Dalhousie University, Canadá
(Inglês). Tradução: junho 2011
Introdução
Nossos programas de vacinação de crianças pequenas são uma das realizações mais importantes do século XX em matéria de saúde pública. Eles mudaram a imagem da infância – literalmente salvando a vida de milhares de crianças a cada ano e minimizando ou eliminando os riscos de diversas doenças graves em bebês e crianças.1,2 Com exceção da água potável, nenhuma outra modalidade, nem mesmo a dos antibióticos, teve impacto tão importante sobre a redução da mortalidade, nem provocou tanta melhoria nas condições de sobrevivência.3
Do que se trata
Calendário de vacinação recomendado
No Canadá, o National Advisory Committee on Immunization (NACI) (Comitê Nacional Consultivo sobre Vacinação) fornece continuamente ao governo federal – ou seja, ao Departamento de Saúde – orientação adequada nas áreas médica, científica e de saúde pública sobre vacinação.1 O calendário de vacinação recomendado atualmente pelo NACI para as crianças está resumido na Tabela 1.1,4 Uma vez que no Canadá a responsabilidade pelo atendimento à saúde cabe às províncias, e não ao governo federal, cada província e cada território decidem individualmente a inclusão de vacinas específicas nos programas de vacinação que financiam, quais vacinas serão incluídas e em que momento.5 Lamentavelmente, essa abordagem resultou em uma cobertura desigual e discrepante dos programas de vacinação de crianças em nosso país.5,6 Por exemplo, em dezembro de 2003, o NACI recomendou novas vacinas – entre elas, a vacina contra catapora,7 a conjugada contra o pneumococo,8 a conjugada contra o meningococo 9 e a vacina contra coqueluche acelular para adolescentes10 (ver adiante) –, disponíveis em programas de rotina em alguns territórios e províncias.6 Apesar de inúmeras solicitações, ainda não dispomos no Canadá de uma Estratégia Nacional de Vacinação, ao contrário do que ocorre nos Estados Unidos, na Austrália, no Reino Unido e em outros países.5,6,11-14
Benefícios da vacinação de rotina para crianças pequenas: vidas salvas
Não muito tempo atrás, os pais e os profissionais da área da saúde foram os primeiros a perceber as consequências potenciais de algumas doenças para os bebês e as crianças pequenas que contraíam doenças que hoje são evitadas por programas de vacinação de rotina. Por volta de 1900, cinco em cada mil crianças nascidas no Canadá e nos Estados Unidos morriam devido à coqueluche antes de completar 5 anos de idade;15 e a difteria – doença bacteriana que impede a deglutição e a respiração – era uma das causas mais comuns de mortalidade infantil entre um e 5 anos de idade, matando milhares de crianças a cada ano.1 A poliomielite – doença viral infecciosa que afeta o sistema nervoso central – era uma calamidade muito temida, comum no período do verão, causa frequente de morte ou de deficiência física.16 A Tabela 2 compara a prevalência das doenças antes e depois da introdução das vacinas de rotina.1,2,8-10,15-18
Para que as crianças possam tirar proveito dos benefícios dessas vacinas, é preciso não só que recebam as vacinas, mas também que as recebam a tempo. Embora tenhamos acesso a cuidados intensivos modernos à base de antibióticos, essas doenças ainda podem matar ou causar deficiência.19-21 Em meados da década de 1990, muitas famílias da Federação Russa voltaram a enfrentar o perigo da difteria e constataram a importância da vacinação: a doença ressurgiu com força e foram registrados 115 mil casos e três mil mortes.20 Essa epidemia ocorreu em um país em que a difteria já havia sido bem controlada. A dissolução da antiga União Soviética ocasionou profundas mudanças sociais, entre as quais uma drástica redução nas taxas de vacinação de bebês e de crianças e uma incapacidade de fornecer doses de reforço para adultos. Os estudos de casos-controle mostraram que os indivíduos vacinados estavam protegidos e aqueles que não haviam recebido as vacinas corriam risco.22 Essa trágica epidemia não foi causada por uma deficiência da vacina, e sim pela deficiência em sua aplicação.
Problemas
As vacinas causam menos efeitos adversos do que as doenças
O Quadro 3 apresenta os efeitos da doença e os efeitos adversos colaterais conhecidos das vacinas que, aplicadas de forma rotineira, podem evitar doenças em bebês e crianças pequenas.1,8-10,15-17 De modo geral, todas essas doenças são graves e podem ser fatais, ao passo que os efeitos adversos associados às vacinas, quando se manifestam, normalmente não são graves: desconforto localizado e/ou inflamação no local da injeção e/ou febre baixa ou irritação na pele. A pesquisa demonstrou que é possível reduzir a dor localizada de uma vacina intramuscular de DTP/VIP/Hib por meio do uso tópico de uma mistura de lidocaína e de prilocaína, sem afetar negativamente o desenvolvimento da resposta de proteção da vacina polivalente.23 No caso de bebês, a dor provocada pela aplicação de diversas injeções em uma mesma consulta pode ser amenizada por meio de sacarose oral ou de estimulação tátil oral (mamadeira ou chupeta), ou ainda mantendo a criança no colo.24
É possível que ocorram efeitos adversos graves associados às vacinas de rotina, mas são muito mais raros do que os efeitos graves associados às doenças.1,2,8-10,15-17 A meningite asséptica, por exemplo – uma infecção das membranas e do fluido que reveste o cérebro e a medula espinhal –, ocorre em 5% dos pacientes que têm caxumba – uma doença viral que provoca o inchaço das glândulas salivares do queixo e do rosto –, e a proporção desses pacientes que podem adquirir surdez permanente chega a 0,5%.1,2 Por outro lado, a meningite asséptica consecutiva à vacina contra a caxumba com a cepa Jeryl Lynn – o tipo de cepa de vacina viral modificada e diluída contra a caxumba, que é utilizado no Canadá e em diversos outros países – só ocorre em menos de uma em 800 mil doses, e essa proporção pode chegar a somente uma em três milhões de doses.2,25 Além disso, a meningite asséptica associada à vacina não acarreta problemas permanentes, como a surdez.25
Além desses efeitos adversos graves conhecidos, porém raros, associados às vacinas (Tabela 3), alega-se que vacinas ministradas periodicamente aos bebês podem causar outros problemas graves, como SMSB – síndrome de morte súbita do bebê –26 e autismo.27 Entretanto, a pesquisa demonstrou que essas alegações não têm fundamento.28-31 Não há relação causal entre a vacinação do bebê e a síndrome da morte súbita do bebê ou o autismo. Embora tenham sido constatados incidentes logo após a administração de uma vacina ao bebê – isto é, estabelecendo-se uma possível relação temporal –, a administração da vacina não foi a causa do problema.32,33
Em 1994, o Departamento de Saúde do Canadá instituiu o Advisory Committee on Causality Assessment (ACCA) (Comitê Consultivo sobre Avaliação de Causalidade), para examinar os relatos sobre efeitos adversos graves associados às vacinas no Canadá.33 Esse comitê de especialistas tem a tarefa de fiscalizar a segurança das vacinas. Examina regularmente todos os relatos que se referem a efeitos adversos graves e não habituais associados às vacinas, a fim de determinar, com base em uma abordagem sistemática e padronizada, se a associação do evento à aplicação da vacina tende a ser causal, é provavelmente causal, é possivelmente causal, tende a ser não causal, não existe ou não permite classificação.33 Em nível internacional, a Organização Mundial da Saúde criou, em 1999, o Comitê Consultivo Mundial sobre Segurança de Vacinas, cuja tarefa é dar respostas imediatas, eficientes e com rigor científico a questões relacionadas à segurança das vacinas que possam ter relevância em termos globais.34
Em 1991, o Departamento de Saúde do Canadá, com a participação da Sociedade Canadense de Pediatria e de outros colaboradores, criou uma rede de vigilância pediátrica abrangendo todo o país, com base em hospitais infantis e estabelecida em cinco centros. O objetivo era aprimorar a detecção de eventos adversos graves associados a vacinas e falhas de vacinas, e identificar doenças infecciosas que afetam bebês e crianças e que já são evitáveis ou estão prestes a se tornar evitáveis por meio de vacinas. Em 1995, a rede foi ampliada para 11 centros e, em 1999, para 12 centros.35-37 Os dados compilados pela rede confirmaram, recorrentemente, que as vacinas de rotina para crianças pequenas são muito seguras.38 Além disso, a rede IMPACT mostrou-se muito útil para detectar efeitos adversos graves raros, porém inesperados – por exemplo, infecções generalizadas pelo bacilo Calmette-Guérin (BCG) em bebês aborígenes que receberam a vacina BCG39 –, o que levou a uma reavaliação da política.40 A rede IMPACT também conseguiu demonstrar uma queda acentuada na ocorrência da doenças após a introdução de uma nova vacina41 e uma redução dos efeitos adversos após a troca para uma vacina nova, aperfeiçoada.42
Contexto de pesquisa
Melhores práticas para programas de vacinação
Em 1995, o NACI deu início a um processo consultivo com dois anos de duração a fim de desenvolver diretrizes para a vacinação de crianças que fossem aplicáveis aos sistemas de vacinação privado e público no Canadá. A Tabela 4 fornece uma visão resumida dessas diretrizes.1 A pesquisa demonstrou que diversos fatores podem melhorar as taxas de vacinação, entre os quais lembretes em momentos adequados, a qualidade do material educativo destinado aos pais, atendimento em clínicas após o horário habitual e aos finais de semana, monitoramento da vacinação, aplicação de diversas vacinas em uma única consulta, regulamentação para vacinas, educação multidisciplinar do profissional e eliminação de obstáculos financeiros à vacinação.1,5,6,11, 43-47
No que diz respeito à aceitação da vacina, a pesquisa mostrou que, para os pais, o que importa é receber a informação necessária para tomar uma decisão esclarecida,46,48-50 qualquer que seja a forma como essa informação é transmitida.49 A edição 2002 do Guia Canadense da Vacinação do NACI levou em consideração esse aspecto, e acrescentou um capítulo separado sobre as questões da aceitação e das preocupações dos pais em relação à vacinação, para ajudar os profissionais envolvidos na vacinação a lhes orientarem melhor.1 Reconhecendo que as informações sobre vacinas contidas no Guia Canadense de Vacinação do NACI podiam ser demasiadamente técnicas para os pais, a Sociedade Canadense de Pediatria apoiou o desenvolvimento de um manual especialmente concebido para eles, intitulado Your Child’s Best Shot, publicado pela primeira vez em 1997, e atualizado posteriormente para incluir as vacinas recomendadas pelo NACI em 2002.2
Como observado anteriormente, profissionais da área da saúde bem-informados constituem um fator importante para o aumento das taxas de vacinação. Entretanto, a pesquisa demonstrou que muitos deles são deficientes nesse aspecto.45,46,50,51 Os esforços para superar essa falta de conhecimento incluem a renovação e a atualização do Guia Canadense da Vacinação, do NACI; educação continuada sobre as vacinas para médicos e enfermeiros; artigos em revistas; novas pesquisas; criação da Coalizão Canadense para Conscientização e Promoção da Vacinação;52 criação da Associação Canadense para Pesquisa e Avaliação da Vacinação;53 e a realização, duas vezes por ano, de uma Conferência Nacional sobre Vacinação.54
Programas de vacinação para crianças pequenas com necessidades especiais
Embora o calendário de vacinação de rotina do NACI (Tabela 1) seja apropriado para a maioria das crianças canadenses, há subgrupos com necessidades especiais, que incluem:
- bebês e crianças pequenas nascidos no exterior que chegam ao Canadá como imigrantes, refugiados, estrangeiros adotados, que talvez não tenham recebido todas as vacinas recomendadas no país e que talvez não possuam a documentação adequada relativa à vacinação;
- bebês prematuros;
- bebês e crianças com imunodeficiências congênitas ou causadas por alguma doença;
- bebês e crianças com coagulopatias ou com taxa de coagulação não funcional ou ausente;
- bebês e crianças que viajam para outros países.1
- Em cada um desses casos, é possível que as exigências em termos de vacinação e os calendários de aplicação precisem ser adaptados.1,55,56
Resultados de pesquisas recentes
Novas vacinas recomendadas pelo NACI para crianças pequenas
Três vacinas que recentemente passaram a ser recomendadas pelo NACI para bebês e crianças pequenas ainda não são incluídas em todos os territórios e províncias por programas de vacinação subvencionados.6 Entre elas estão as vacinas contra catapora,7 conjugada contra o pneumococo, para prevenir a infecção sanguínea, a pneumonia e a meningite causadas por essa bactéria,8 e a vacina conjugada contra o meningococo, para prevenir a meningite e a infecção sanguínea causadas pelo meningococo.9 Os riscos dessas doenças, os benefícios das vacinas e seus efeitos colaterais estão resumidos nas Tabelas 2 e 3. Nos três casos, ficou demonstrado que essas vacinas são seguras e efetivas para prevenir doenças graves em bebês e crianças pequenas, mas cada uma delas é também relativamente cara em comparação com as vacinas “regulares” para bebês.57 Os custos proibitivos dessas vacinas levaram a atrasos e disparidades em sua inclusão na lista de vacinas “de rotina” cobertas em cada província e território.5,6,47 Problema semelhante ocorre em relação à vacina contra coqueluche acelular para adolescentes e adultos. Embora no Canadá essa vacina esteja disponível para bebês e crianças pequenas, a disponibilidade da mesma para adolescentes e adultos ainda não é regular em todo o país, apesar das recomendações do NACI. A utilização generalizada dessa vacina em adolescentes e adultos pode diminuir os eventos de coqueluche nas famílias e, com isso, reduzir a exposição de bebês que ainda não têm idade para receber a vacina – ou seja, aqueles com menos de 6 semanas de idade –, que constituem o grupo com maior risco de mortalidade provocada pela doença.58
Conclusões
As vacinas recomendadas para crianças pequenas são meios seguros e efetivos de eliminar ou reduzir os riscos de muitas doenças graves nos primeiros anos de vida e durante a infância. Bebês e crianças que não recebem as vacinas continuam correndo risco. O Guia Canadense da Vacinação1 do NACI é a melhor fonte de informação e a mais detalhada no que se refere a todos os aspectos da vacinação para os profissionais da área da saúde; e o manual Your Child’s Best Shot2 fornece informações de qualidade para os pais.
Implicações
Para que seja possível melhorar a equidade no acesso a todas as vacinas recomendadas pelo NACI, é preciso que seja estabelecido no país um Programa Nacional de Vacinação para bebês e crianças pequenas, o que permitiria proteger todas as nossas crianças dos danos potenciais ocasionados por uma doença que pode ser evitada pela vacinação. Se a equidade de acesso não for garantida, muitos bebês e crianças continuarão correndo risco de enfrentar problemas como a surdez decorrente da meningite causada pela infecção por pneumococo, além de suas graves implicações ligadas ao desenvolvimento. Os formuladores de políticas nos níveis federal, provincial e territorial devem trabalhar em conjunto para garantir a implementação de um Programa Nacional de Vacinação para bebês e crianças canadenses, de modo que todos tenham acesso às vacinas recomendadas pelo NACI.
TABELA 1
Tabela 1. Calendário de vacinação recomendado pelo NACI para bebês e crianças (referências 1, 8-10, 15-18)
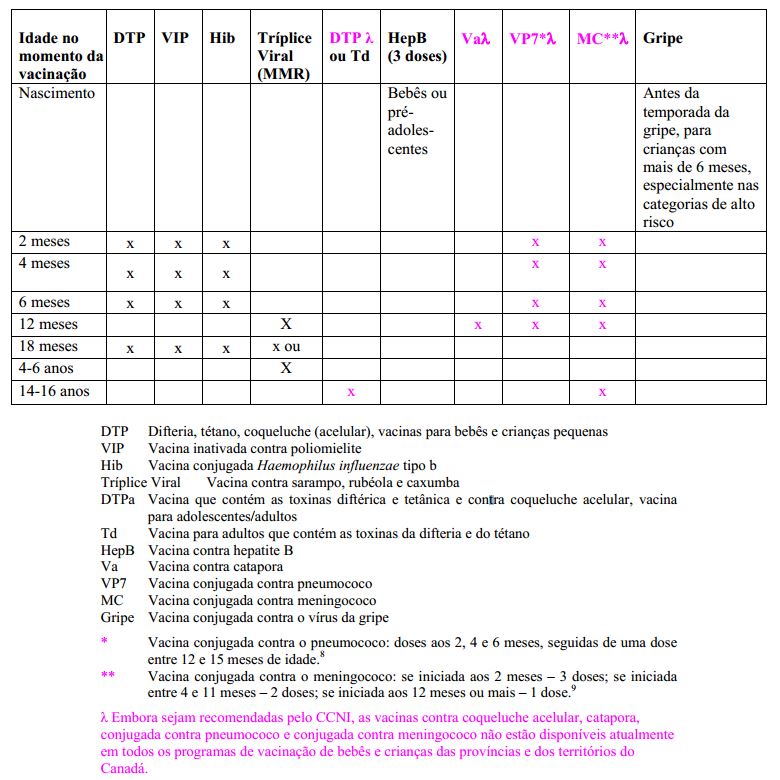
TABELA 2
Doenças graves em bebês, crianças e jovens no Canadá nos períodos pré e pós-vacinação (segundo as referências 1, 2, 8-10, 15-18)
| Disease/ Organism | Incidence Before Vaccination | Incidence After Vaccination |
|---|---|---|
|
Poliomielite 3 tipos de vírus da poliomielite |
2,5 a 28,3/100 mil Epidemia: até 20 mil casos de paralisia. |
Doença erradicada no Canadá e na maioria dos países do mundo. |
| Difteria |
Em 1924, 9 mil casos relatados. Principal causa de óbito de crianças de 1 a 5 anos de idade |
Nenhum caso relatado desde 1996 e apenas 2 a 5 por ano antes dessa data. |
|
Tétano |
60 a 75 casos por ano, 40 a 50 óbitos. |
Menos de 2 casos por ano ao longo dos últimos 15 anos. |
| Coqueluche |
Mais de 150/100 mil casos por ano e entre 50 a 100 óbitos. |
10/100.000 mil casos por ano e 1 a 3 óbitos entre bebês de tenra idade. |
| Haemophilus influenzae typo b |
2 mil casos por ano, sendo 1.500 em crianças com menos de 5 anos. Principal causa de meningite bacteriana em bebês. |
Menos de 50 casos por ano. Causa rara de meningite bacteriana em bebês. |
| Sarampo |
Epidemias cíclicas a cada 2 ou 3 anos. 300 mil a 400 mil casos por ano. |
Atualmente menos de 400 casos por ano. |
| Caxumba |
Cerca de 30 mil casos relatados por ano, porém um número muito maior de casos não relatados. |
Mais de 500 casos por ano. |
| Rubéola |
Cerca de 250 mil casos por ano, e mais de 200 casos anuais de síndrome da rubéola congênita (SRC). |
Menos de 100 casos por ano, 1 a 2 casos anuais de síndrome da rubéola congênita (SRC). |
| Gripe |
Epidemias anuais, infectando até 20% da população. Grande variação de incidência anual. Última erupção importante: 1968, com 50 milhões de casos e 33 mil óbitos. |
Como o vírus da gripe muda a cada ano, torna-se necessária uma vacinação anual. O programa atual visa às pessoas que correm risco elevado e oferece doses em quantidades limitadas para as pessoas com menor risco. Se a vacinação na comunidade for adequada, o potencial de prevenção da doença situa-se entre 70% e 90%, se houver imunocompetência. Se não for adequada, protege somente entre 30% e 60% da população vacinada. Menos efetiva caso não seja imunocompetente. |
| Hepatite B |
20 mil novas infecções por ano, 1 pessoa em cada 200 é portadora crônica. A CB (Colúmbia Britânica, terceira maior província canadense) teve uma taxa de 33,7/100 mil em 1992. O risco de transmissão de uma mãe infectada para seu bebê recém-nascido é de 90%. |
De 1992 a 2002, na CB, após a adoção de um programa de vacinação de estudantes da 6ª série, a taxa geral de infecção aguda caiu de 7 para 2/100 mil; entre indivíduos de 12 a 21 anos, caiu de 1,7 para 0/100 mil. A vacinação de bebês recém-nascidos evita a transmissão pela mãe em >90% dos casos. |
| Catapora |
Infecção em 50% das crianças aos 5 anos e 90% das crianças aos 12 anos de idade. |
Nos Estados Unidos, com o programa nacional e as taxas de cobertura de 80% das crianças menores de 3 anos, os óbitos que podem ser atribuídos à catapora diminuíram em 76%. |
| Streptococcus pneumoniae |
Cerca de 500 mil casos anuais de doenças causadas por pneumococo, sendo mais de 200 mil em crianças menores de 5 anos. Taxas de infecções invasivas causadas por estreptococo |
A vacina conjugada heptavalente para bebês só foi autorizada no Canadá em 2001. Nos Estados Unidos, ensaios clínicos em bebês mostraram uma taxa de eficácia da vacina de 94% para doenças invasivas, devido a cepas das vacinas e de 89% para doença invasiva devido a qualquer cepa de pneumococo. |
|
Neisseria meningitidis |
Endêmica no Canadá, com novas epidemias a cada 10 a 15 anos. 200 a 300 casos endêmicos por ano. As taxas nos 3 grupos etários mais elevados são: Serogrupos em 2001: |
A vacina conjugada do grupo C para bebês só foi autorizada no Canadá em 2001. No Reino Unido, a vacinação de rotina para bebês começou em 1999 com uma campanha de acompanhamento para crianças e adolescentes que reduziu a doença em >90%. |
TABELA 3
Comparação dos efeitos das doenças graves no bebê e na criança e dos efeitos adversos das vacinas (referências 1, 2, 8-10, 15-17)
| Disease / Organism | ||
|
Poliomielite |
4 a 8% têm doença de pouca importância, 1% têm poliomielite paralítica grave, 1 paciente hospitalizado em cada 20 morre, e em 50% dos pacientes a paralisia torna-se permanente. |
Desconforto ou vermelhidão no local da injeção em 5% dos sujeitos. Vacina inativada, portanto não há risco de poliomielite associado à vacina. |
|
Difteria |
Ocorrência de óbito em 5 a 10% dos casos, mesmo tratados em UTI com antitoxinas e antibióticos. A toxina pode provocar complicações neurológicas e cardíacas. |
Vacina DTP: desconforto, inchaço ou vermelhidão no local da injeção em 20% dos sujeitos; febre em 5% dos sujeitos. Um nódulo passageiro pode surgir no local da injeção e perdurar algumas semanas. Cerca de 70% apresentam vermelhidão e inchaço no reforço aos 4-6 anos. |
|
Tétano |
Ocorrência de óbito em 5% a 10% dos casos, mesmo com tratamento em UTI, com antitoxinas e antibióticos. O risco é maior para crianças muito pequenas e pessoas de idade muito avançada. |
Ver acima o que diz respeito à DTP. As reações localizadas aumentam com a idade, principalmente entre os adultos que recebem uma dose de reforço. São raros os relatos de sequelas no nervo periférico (<1/1 milhão). |
|
Coqueluche |
Óbito de 1/400 bebês com coqueluche, 1/400 sofre danos cerebrais permanentes. Entre as crianças menores de 6 meses, 1% morre de pneumonia ou de privação fatal de oxigênio no cérebro. |
Idem acima para DTP. |
|
Haemophilus influenzae tipo b |
Óbito em 5% dos casos de meningite; danos cerebrais permanentes em 10% a 15% dos casos; surdez em 10% a 20% dos casos. |
Normalmente combinada, como no caso de DTP/VIP/Hib. Sobre efeitos colaterais (idênticos aos da DTP), ver acima. |
|
Sarampo |
10% apresentam complicações como pneumonia e infecções no ouvido. 1/1 mil apresenta encefalite (infecção do cérebro); 10% de óbitos; 25% com danos cerebrais permanentes; 1/25 mil com panencefalite esclerosante subaguda (PES) (doença cerebral degenerativa fatal que se manifesta mais tarde). |
Geralmente combinada, como a Tríplice Viral. 5% a 10% sentem desconforto ou inchaço localizado e febre, com ou sem rash cutâneo. 1/24 mil tem taxa baixa de plaquetas. <1/1 milhão tem encefalite. |
|
Caxumba |
1/20 desenvolve meningite asséptica (infecção viral dos tecidos e fluidos que envolvem o cérebro). 1/200 desenvolve uma encefalite. Surdez em 1/200 mil. Inflamação dos testículos em 20% a 30% dos sujeitos do sexo masculino; inflamação dos ovários em 5% das mulheres pós-púberes. |
Desconforto localizado, inchaço e vermelhidão ou febre em 5 a 10% dos casos. |
|
Rubéola |
50% têm rash cutâneo, glândulas inchadas, febre; 50% dos adolescentes e dos adultos desenvolvem artrite e artralgia; 1/6 mil tem encefalite. Nas 10 primeiras semanas de gravidez, 85% de risco de síndrome da rubéola congênita que causa morte do feto, surdez, cegueira e/ou doença coronariana. |
10% apresentam desconforto localizado e febre, 5% têm inchaço nas glândulas, artralgia (principalmente adultos) e rigidez no pescoço. 1% desenvolve rash cutâneo não infeccioso. |
|
Gripe |
As taxas de mortalidade mais elevadas registram-se entre pessoas com mais de 65 anos e crianças com menos de 1 ano de idade. Complicações: pneumonia, crises febris, encefalite, miocardite, miosite, encefalite viral, síndrome de Reyes. |
Reações leves no local da injeção e/ou febre baixa durante 1 a 3 dias em 60% dos sujeitos. Ocasionalmente, síndrome óculo-respiratória leve. Raramente: síndrome de Guillain-Barré, 1/1 milhão |
|
Hepatite B |
Variável: doença hepática que vai de assintomática a devastadora. Assintomática em recém-nascidos; de 5% a 15% das crianças entre 1 e 5 anos de idade têm alguns sintomas; 33% a 50% das crianças maiores de 5 anos têm náuseas, icterícia, febre, vômitos e inchaço no fígado e no baço. < 1% têm falência hepática fulminante e mortal. Doença crônica em 90% dos bebês, 25% a 50% das crianças de 1 a 5 anos e 6% a 10% das crianças mais velhas. Risco de câncer no fígado, falência hepática e doença crônica. |
15% sentem desconforto localizado e ocasionalmente têm febre baixa. |
|
Catapora |
Taxas de mortalidade de 1 a 3/100 mil casos em crianças. Complicações em 5% a 10% das crianças que anteriormente gozavam de boa saúde: pneumonia, encefalite (1/5 mil), ataxia cerebelar (1/4 mil), osteomielite, hepatite, artrite séptica. Em 50% das crianças que têm uma infecção causada por fascite necrosante, a catapora precede essa doença. Herpes zóster em adultos. Síndrome congênita da catapora. |
15% a 20% têm inchaço leve, desconforto no local da injeção e/ou febre. 1% a 5% têm rash cutâneo leve. |
|
Streptococcus pneumoniae |
Principal causa de doença bacteriana invasiva em crianças pequenas. Número de casos por ano: 65 meningites (perda de audição 20% a 30%, danos cerebrais 15% a 20%), 700 casos de bacteremia (septicemia), 2.200 casos de pneumonia com necessidade de hospitalização, 9 mil casos de pneumonia sem necessidade de hospitalização. Taxa de óbito: <6 meses 4,3%; 12 anos, 2%. 15 óbitos/ano em crianças menores de 5 anos. O risco de doenças graves é maior para pacientes que sofrem de anemia de hemácias falciformes ou de HIV. <6 meses, 4,3%; 12 anos, 2%. 15 óbitos/ano em menores de 5 anos. O risco de doenças graves é maior para pacientes que sofrem de anemia de hemácias falciformes ou têm HIV. |
Vacina heptavalente bem tolerada por bebês e por crianças pequenas. Reações leves em 10% a 15% dos sujeitos. |
|
Neisseria meningitidis |
Meningite, 30% a 50% (TM 5%); meningite + bacteremia (septicemia), 40%; bacteremia (septicemia), apenas 7% a 10% (TM 20% a 40%). Outras complicações: artrite, pneumonia, peritonite. Taxas de mortalidade: 10%, mesmo com tratamento intensivo/antibióticos. Taxa de mortalidade (TM) mais elevada: <1 ano 1/100 mil. Taxas de mortalidade: 10%, mesmo com tratamento intensivo/antibióticos. Taxa de mortalidade (TM) mais elevada: <1 ano 1/100 mil. |
Bebês/crianças pequenas, vacina C conjugada: leves reações localizadas, menos comuns do que no caso da vacina DTP/VPI/Hib; reações graves são muito raras. |
* A ocorrência de choque anafilático (ou anafilaxia) – uma reação alérgica potencialmente mortal – é rara (de 0,11 a 0,31 casos relatados para 100 mil doses de vacina distribuídas). É mais raro entre bebês e crianças pequenas, produzindo-se nos 30 minutos seguintes à aplicação da vacina. Pode ser tratado com injeção de epinefrina (adrenalina).
TABELA 4
Diretrizes nacionais para a prática de vacinação das crianças: resumo*
| 1 |
Os serviços de vacinação devem estar prontamente disponíveis |
| 2 |
Não deve haver nenhum obstáculo nem pré-requisitos desnecessários para a aplicação das vacinas. |
| 3 |
Os profissionais envolvidos devem aproveitar todas as consultas para detectar as necessidades em termos de vacinação e, quando indicado, devem vacinar as crianças. |
| 4 |
Os profissionais envolvidos devem fornecer aos pais informações gerais sobre a vacinação. |
| 5 |
Os profissionais envolvidos devem informar os pais, de maneira clara, sobre os riscos e os benefícios das vacinas que seu filho vai receber. |
| 6 |
Os profissionais envolvidos somente devem recomendar o adiamento ou a suspensão da administração das vacinas em casos de real contra-indicação. |
| 7 |
Os profissionais envolvidos devem administrar todas as doses de vacinas indicadas para a criança por ocasião de cada consulta. |
| 8 |
Os profissionais envolvidos devem certificar-se de que todas as aplicações de vacinas sejam cuidadosamente registradas. |
| 9 |
Os profissionais envolvidos devem manter resumos dos registros de vacinação facilmente acessíveis, para facilitar a vacinação adequada à idade. |
| 10 |
Os profissionais envolvidos devem relatar imediatamente efeitos adversos clinicamente importantes da vacinação, de maneira precisa e detalhada. |
| 11 |
Os profissionais envolvidos devem relatar todos os casos de doenças que podem ser evitadas por meio de vacinas, na forma determinada pela legislação local. |
| 12 |
Os profissionais envolvidos devem adotar procedimentos adequados de gestão da vacinação. |
| 13 |
Os profissionais envolvidos devem manter protocolos atualizados e facilmente acessíveis em todos os locais onde as vacinas são administradas. |
| 14 |
Os profissionais envolvidos devem receber capacitação adequada e educação continuada sobre recomendações atualizadas para a vacinação. |
| 15 |
Os profissionais envolvidos devem operar um sistema de monitoramento. |
| 16 |
Devem ser realizadas auditorias em todos os centros de vacinação, para avaliar a qualidade dos relatos e os níveis de cobertura da vacinação. |
*Adaptado a partir do Guia Canadense da Vacinação, 6a edição.1
Referências
- National Advisory Committee on Immunization. Canadian Immunization Guide. 6th ed. Ottawa, Ontario: Health Canada; 2002.
- Gold R. Your child’s best shot: a parent’s guide to vaccination. 2nd ed. Ottawa, Ontario: Canadian Paediatric Society; 2002.
- Plotkin SL, Plotkin SA. A short history of vaccination. In: Plotkin SA, Orenstein WA, eds. Vaccines. 3rd ed. Philadelphia, Pa: WB Saunders Co; 1999:1-12.
- Division of Immunization and Respiratory Diseases. Population and Public Health Branch. Health Canada. Immunization Schedule.
- Naus M, Scheifele DW. Canada needs a national immunization program: an open letter to the Honourable Anne McLellan, federal minister of health. CMAJ - Canadian Medical Association Journal 2003;168(5):567-568.
- Infectious Diseases and Immunization Committee, Canadian Paediatric Society. Routine immunization schedule: Update 2004. Peadiatric Child Health 2004;9(1):17-20.
- National Advisory Committee on Immunization. Update on varicella. CCDR - Canadian Communicable Disease Report 2004;30(ACS-1):1-28.
- National Advisory Committee on Immunization. Statement on recommended use of pneumococcal conjugate vaccine. CCDR – Canada Communicable Disease Report 2002;28(ACS-2):1-32.
- National Advisory Committee on Immunization. Statement on recommended use of meningococcal vaccines. CCDR – Canada Communicable Disease Report 2001;27(ACS-6):2-36.
- National Advisory Committee on Immunization. Prevention of pertussis in adolescents and adults. CCDR – Canada Communicable Disease Report 2003;29(ACS-5):1-9.
- Lynk A. A call to arms (and legs): Implement the National Immunization Strategy. Peadiatrics and Child Health 2002;7(2):615-616.
- Romanow RJ, commisionner. Building on values: The future of health care in Canada. Final report. Saskatoon, Saskatchewan: Commission on the Health Care in Canada; 2002.
- National Immunization Strategy. In: Budget 2003. Investing in Canada’s Health Care System. Canada: Department of Finance; 2003:15.
- National Advisory Committee on SARS and Public Health. Learning from SARS - Renewal of public health in Canada. Ottawa: Health Canada; 2003.
- Cherry JD, Brunell PA, Golden GS, Karson DT. Report of the task force on pertussis and pertussis immunization. Pediatrics 1988;81(suppl):939-984.
- Rutty CJ. The middle-class plague: epidemic polio and the Canadian state, 1936-1937. Bulletin Canadien d'Histoire de la Medecine / Canadian Bulletin of Medical History 1996;13(2):277-314.
- Patrick DM, Bigham M, Ng H, White R, Tweed A, Skowronski DM. Elimination of acute hepatitis B among adolescents after one decade of an immunization program targeting Grade 6 students. Pediatric Infectious Disease Journal 2003;22(10):874-877.
- Immunization and Respiratory Infections Division, Centre for Infectious Disease Prevention and Control. Enhanced surveillance of invasive meningococcal disease in Canada: 1 January, 1999, through 31 December, 2001. CCDR - Canada Communicable Disease Report 2004;30(3):17-28.
- Samba E, Nkrumah F, Leke R. Getting polio eradication back on track in Nigeria. New England Journal of Medicine 2004;350(7):645-646.
- Markina SS, Maksimova NM, Vitek CR, Bogatyreva EY, Monisov AA. Diphtheria in the Russian Federation in the 1990s. Journal of Infectious Diseases 2000;181(Suppl 1):S27-S34.
- Grewal S, Scheifele D. Haemophilus influenzae type b disease at 11 pediatric centres, 1996-1997. CCDR - Canada Communicable Disease Report 1998;24(13):105-108.
- Bisgard KM, Rhodes P, Hardy IRB, Litkina IL, Filatov NN, Monisov AA, Wharton M. Diphtheria toxoid vaccine effectiveness: A case controlled study in Russia. Journal of Infectious Diseases 2000;181(Suppl 1):S184-S187.
- Halperin BA, Halperin SA, McGrath P, Smith B, Houston T. Use of lidocaine-prilocaine patch to decrease intramuscular injection pain does not adversely affect the antibody response to diphtheria-tetanus-acellular pertussis-inactivated poliovirus-Heamophilus influenzae type b conjugate and hepatitis B vaccines in infants from birth to six months of age. Pediatric Infectious Disease Journal 2002;21(5):399-405.
- Reis EC, Roth EK, Syphan JL, Tarbell SE, Holubkov R. Effective pain reduction for multiple immunization injections in young infants. Archives of Pediatrics and Adolescent Medicine 2003;157(11):1115-1120.
- Plotkin SA, Wharton M. Mumps Vaccine. In: Plotkin SA, Orenstein WA, eds. Vaccines. 3rd ed. Philadelphia, Pa: WB Saunders Co.; 1999:279-281.
- Baraff LJ, Ablon WJ, Weiss RC. Possible temporal association between diphtheria-tetanus toxoid-pertussis vaccination and sudden infant death syndrome. Pediatric Infectious Disease Journal 1983;2(1):7-11.
- Wakefield AJ, Murch SH, Anthony A, Linnell J, Casson DM, Malik M, Berlowitz M, Dhillon AP, Thomson MA, Harvey P, Valentine A, Davies SE, Walker-Smith JA. Ileal-lymphoid-nodular hyperplasia, non-specific colitis, and pervasive developmental disorder in children (Retracted article. See vol 363, pg 750, 2004). Lancet 1998;351(9103):637-641.
- Howson CP, Howe CJ, Fineberg HV, eds; Committee to Review the Adverse Consequences of Pertussis and Rubella Vaccines, Institute of Medicine. Adverse effects of pertussis and rubella vaccines. Washington, DC: National Academies Press; 1991.
- Strauss B, Bigham M. Does measles-mumps-rubella (MMR) vaccination cause inflammatory bowel disease and autism? CCDR - Canada Communicable Disease Report 2001;27(8):65-72.
- Stratton K, Gable A, Shetty P, McCormick M, eds. Immunization Safety Review: Measles-Mumps-Rubella Vaccines and Autism. Washington, DC: Institute of Medicine, National Academies Press; 2001.
- Wilson K, Mills E, Ross C, McGowan J, Jadad A. Association of autistic spectrum disorder and the measles, mumps and rubella vaccine. A systematic review of current epidemiological evidence. Archives of Pediatrics and Adolescent Medicine 2003;157(7):628-634.
- Stratton KR, Howe CJ, Johnston RB, eds. Adverse Events Associated with Childhood Vaccines. Evidence Bearing on Causality. Washington, DC: Institute of Medicine. National Academies Press; 1994.
- Collett JP, MacDonald N, Cashman N, Pless R, Advisory Committee on Causality Assessment. Monitoring signals for vaccine safety: the assessment of individual adverse event reports by an expert advisory committee. Bulletin of the World Health Organization 2000;78(2):178-185.
- World Health Organization. Global Advisory Committee on Vaccine Safety (GACVS).
- Canadian Paediatric Society. IMPACT - Immunization Monitoring Program - ACTive.
- Morris R, Halperin SA, Dery P, Mills E, Lebel M, MacDonald N, Gold R, Law B, Jadavji T, Scheifele DW, Marchessault V, Duclos P: IMPACT monitoring network: A better mousetrap. Canadian Journal of Infectious Diseases 1993;4(4):194-195.
- Scheifele DW, Halperin SA, CPS/Health Canada, Immunization Monitoring Program, Active (IMPACT). Immunization Monitoring Program, Active: a model of active surveillance of vaccine safety. Seminars in Pediatric Infectious Diseases 2003;14(3):213-219.
- Scheifele DW, Halperin SA, Gold R, Samson H, King A, Canadian Paediatric Society/Health Canada Immunization Monitoring Program, ACtive (IMPACT). Assuring vaccine safety: a celebration of 10 years of progress with the IMPACT project. Paediatrics and Child Health 2002;7(9):645-648.
- Scheifele D, Law B, Jadavji T, on behalf of IMPACT. Disseminated Bacille Calmette-Guerin Infection: Three recent Canadian cases. CCDR - Canada Communicable Disease Report 1998;24(9):69-75.
- Elwood K. Bacille Calmette-Guérin vaccination. In: Long R, ed. Canadian Tuberculosis Satandards. 5th ed. Ottawa, Ontario: Health Canada, Canadian Lung Association; 2000: 223-228.
- Scheifele D, Halperin S, on behalf of IMPACT. Haemophilus influenzae type b disease control using Pentacel, Canada, 1998-1999. CCDR - Canada Communicable Disease Report 2000;26(11):93-96.
- Le Saux N, Barrowman NJ, Moore DL, Whiting S, Scheifele D, Halperin S, for Members of the Canadian Paediatric Society/ Health Canada Immunization Monitoring Program–Active (IMPACT). Decrease in hospital admissions for febrile seizures and reports of hypotonic-hyporesponsive episodes presenting to hospital emergency departments since switching to acellular pertussis vaccine in Canada: a report from IMPACT. Pediatrics 2003;112(5):e348-e348.
- DuPlessis HM, Bell WC, Boulter SC, Cora-Bramble D, Feild C, Handal GA, Katcher ML, Rushton FE, Wood DL, Lavin A, Melinkovich P, Belardo JH, Rodewald LE, Varrasso DA, Mejia CA, Yasuda KE, Hammer LD, Harbaugh NR, Itkin PG, Jakubec PJ, Walker RD, France FL, Herr TJ, Lieberthal AS, Swanson J, Grimm KT, Bien AA, Davis T, Price WS, Sebring RH. Increasing immunization coverage. Pediatrics 2003;112(4):993-996.
- Bjornson GL, Scheifele DW, Lajeunesse C, Bell A. Effect of reminder notices on the timeliness of early childhood immunizations. Paediatrics and Child Health 1999;4(6):403-408.
- Boulianne N, Deceuninck G, Duval B, Lavoie F, Dionne M, Carsley J, Valiquette L, Rochette L, De Serres G. Why are some children incompletely vaccinated at the age of 2? [in French]. Canadian Journal of Public Health. Revue Canadienne de Sante Publique 2003;94(3):218-223.
- de Courval FP, De Serres G, Duval B. Varicella vaccine: factors influencing uptake. Canadian Journal of Public Health. Revue Canadienne de Sante Publique 2003;94(4):268-271.
- Scheifele DW. New vaccines and the rising costs of caring. Paediatrics and Child Health 2000;5(7):371-372.
- Ball LK, Evans G, Bostrom A. Risky buisness: Challenges in vaccine risk communication. Pediatrics 1998;101(3):453-458.
- Bjornson GL, Scheifele DW, Gold R. Assessment of parent education methods for infant immunization. Canadian Journal of Public Health. Revue Canadienne de Sante Publique 1997;88(6):405-408.
- Gust DA, Woodruff R, Kennedy A, Brown C, Sheedy K, Hibbs B. Parental perceptions surrounding risks and benefits of immunization. Seminars in Pediatric Infectious Diseases 2003;14(3):207-212.
- Dionne M, Boulianne N, Duval B, Lavoie F, Laflamme N, Carsley J, Valiquette L, Gagnon S, Rochette L, De Serres G. Lack of conviction about vaccination in certain Quebec vaccinators [in French]. Canadian Journal of Public Health. Revue Canadienne de Sante Publique 2001;92(2):100-104.
- The Canadian Coalition for Immunization Awareness and Promotion / Coalition canadienne pour la sensibilisation et la promotion de la vaccination.
- The Canadian Association for Immunization for Research and Evaluation / Association canadienne pour la recherche et l’évaluation en immunisation.
- Health Canada. Proceedings of the Canadian National Immunization Conference. Canada’s National Immunization Strategy: From Vision to Action. Victoria BC. Dec1-3, 2002. CCDR - Canada Communicable Disease Report 2003;29(S4):1-24.
- Health Canada. Population and Public Health Branch. Travel Medicine Program.
- Children and youth new to Canada: A health care guide. Ottawa, Ontario: Canadian Paediatric Society; 1999.
- Tengs TO, Adams ME, Pliskin JS, Safran DG, Siegel JE, Weinstein MC, Graham JD. Five-hundred life-saving interventions and their cost-effectiveness. Risk Analysis 1995;15(3):369-390.
- Mikelova LK, Halperin SA, Scheifele D, Smith B, Ford-Jones E, Vaudry W, Jadavji T, Law B, Moore D, members of the Immunization Monitoring Program, Active (IMPACT). Predictors of death in infants hospitalized with pertussis: a case-control study of 16 pertussis deaths in Canada. Journal of Pediatrics 2003;143(5):576-581.
Para citar este artigo:
MacDonald NE. Vacinação de rotina em crianças pequenas. Em: Tremblay RE, Boivin M, Peters RDeV, eds. Scheifele DW, ed. tema. Enciclopédia sobre o Desenvolvimento na Primeira Infância [on-line]. https://www.enciclopedia-crianca.com/vacinacao/segundo-especialistas/vacinacao-de-rotina-em-criancas-pequenas. Publicado: Agosto 2004 (Inglês). Consultado em 11 de maio de 2026.
Texto copiado para a área de transferência ✓